研究项目和附属机构
研究兴趣
纳米, 药物输送, 癌症 imaging and 癌症 treatment; gene delivery and gene therapy, 蛋白质/肽交付. 生物材料 in tissue engineering; 组合化学 and drug discovery; High throughput screening; microarrays.
教育
研究抽象
面向临床翻译的工程纳米医学和分子装置
我们研究的动机是发展纳米医学, 分子工具和设备通过基础创新的疾病治疗与临床转化从实验室到床边的目标. 我们的研究是基于共轭化学, 肽化学, 组合化学, polymer chemistry and material chemistry; and our research test beds involve biochemical and molecular biology, 地窖信号和生存能力, 以及用于疾病治疗的动物模型. 我们在分子模拟方面积累了丰富的经验和专业知识, 药理学, 癌症生物学和免疫学治疗发展. 我们对该领域的贡献是开发了一种新颖独特的变革性端突分子纳米平台和一种计算组合方法,以加速基于结构的纳米载体的设计和开发,用于药物的输送, 蛋白质疗法, 还有基因疗法. 该技术已进一步发展为分子装置或功能水凝胶,以减弱致病分子或用于疾病治疗中的局部药物递送, e.g. 癌症, 糖尿病。, 炎症性和自身免疫性疾病, 败血症和其他危急情况(创伤), 燃烧, 心脏手术, 胰腺炎和细胞因子释放综合征, 等.).
I. 基于结构的药物递送纳米载体设计
与游离药物分子相比,纳米药物在疾病治疗中具有减少副作用和提高疗效的特点. 与传统的脂质体/脂质体纳米载体相比, 聚合物纳米颗粒具有多种化学和物理微环境,可用于输送各种类型的药物分子. 然而, 目前的聚合物纳米载体设计仍然遵循经验和“试错”方法(无花果. 1a-I),由于高分子材料的不利特性,e.g. 非均质分子量分布, 化学多样性有限,自组装控制不佳. 高分子纳米药物载体的结构-性能关系的不确定性给临床开发带来了重大风险, 因此, 阻碍了制药行业对纳米药物开发的热情. 一个新兴的可预测的纳米平台对于打破瓶颈和加速纳米医学的发展至关重要.
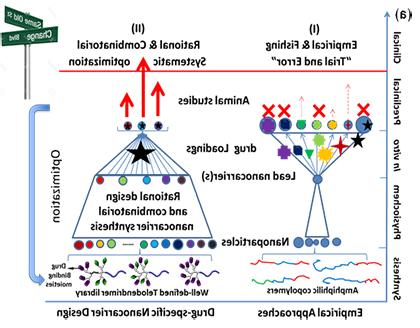
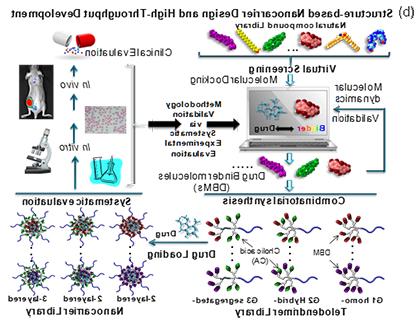
我开发了一种线性树突端突纳米平台, 它有精确的树突结构来装载药物.10-17 采用多肽化学方法构建了端链聚合物, 使模块化设计和结构修改成为可能. 在纳米载体的核心,端突分子的柔性树突结构与药物分子有充分的相互作用, 哪些结构优化可以改善药物包封. 表面两亲性胆酸作为共同构建块的存在确保了纳米颗粒在结构工程中的分散和稳定性. 因此, 我们可以应用计算方法来虚拟筛选分子库,以识别药物结合分子(DBMs)。, 然后可以将其偶联在端突分子的外围,形成一个纳米载体库,以系统地优化给定的药物递送(无花果. 1b). 与传统的“钓鱼方法”(图1 -ⅰ)用于纳米载体的开发, 端突纳米平台提供了一种变革性的, 基于结构的纳米载体优化研究 在活的有机体内 药物输送. 可预测的结构-性能关系, 端突分子纳米平台具有良好的结构和无限的化学多样性,可用于系统优化,符合制药工业治疗发展的标准. 重要的是, 它增加了纳米医学在临床试验之前穿越“死亡谷”的机会, 鉴于最佳的疗效和可预测的纳米药物(图1 a-ii).
许多合理设计的优化纳米载体已经被开发出来,专门用于化学药物的递送, e.g. 紫杉醇、阿霉素、顺铂、SN38、硼替佐米、藤黄酸等. 这些纳米制剂具有优异的载药量(20-100%), w/w), 效率(~ 100%), 稳定性好,粒径小(20~50 nm),可穿透深层组织. 与临床用药相比, 这些纳米制剂降低了药物毒性, 延长PK剖面, 增加肿瘤/炎症的靶向性,显著提高肿瘤治疗和免疫调节治疗的疗效. 其中一些纳米制剂具有巨大的临床转化潜力.
II. 创新的纳米载体设计 原位 肽/蛋白的封装和递送
蛋白质/肽传递系统由于其稳定性差而被高度要求, 不利的PK谱和免疫原性, 等. 基于纳米粒子的蛋白质递送机制仅限于纳米/微粒子中蛋白质的物理纠缠或电荷捕获. 蛋白质变性, 非特异性细胞摄取和有毒化学残留物阻碍了这些方法的应用. 面部递送系统仍未被用于疾病治疗的全身和/或细胞内蛋白质递送.
定制的电荷和疏水构建块可以精确地引入到端枝聚合物(无花果. 2a), 补偿蛋白质表面的电荷和疏水部分以有效地包裹蛋白质 原位 水溶液中. 灵活的“章鱼状”框架通过协同多价杂化电荷和疏水相互作用与蛋白质表面相互作用的构象熵最大化. 考虑到精确的蛋白质结构, 我们可以应用计算方法筛选文库分子来识别蛋白质结合分子(PBMs)。, 它们可以结合在具有不同电荷部分的端突支架上,从而产生一个纳米载体库,以微调蛋白质的装载和释放(无花果. 2b). 表面化学的特殊工程与无污染的生物相容性两性离子材料有效地防止血清蛋白吸附, 蛋白质交换和蛋白质过早释放 在活的有机体内,进一步提高 在活的有机体内 稳定性,并通过微调蛋白质在端枝状分子中的结合亲和力来控制蛋白质释放.
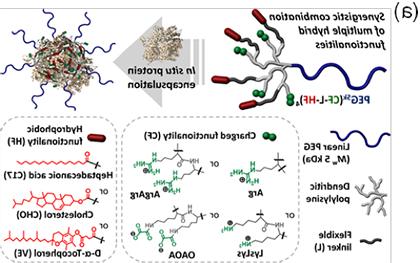
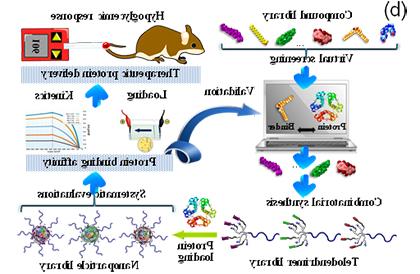
据我们所知,这种杂化的端突蛋白涂层技术是一种无与伦比的 原位 蛋白质包被和封装成小纳米颗粒(10-20 nm)的方法, 在系统和细胞内的蛋白质传递中,是什么维持蛋白质的结构和活性. 我们已经将这种方法应用于设计用于递送各种蛋白质疗法的端突分子纳米载体, 例如, 胰岛素6 and GLP-1 peptide delivery for 糖尿病。 and obesity treatment; cytotoxic proteins (diphtheria toxin7,8、TRAIL蛋白、细胞色素C等.)治疗癌症. 可用于包被抗体, 抗体-药物结合物和重组蛋白,以提高其稳定性和降低免疫原性. 进一步, 该技术为细胞内蛋白质递送提供了一个强有力的工具, 包括抗体和crpr - cas9蛋白复合物, 靶向细胞内通路,直接编辑致病基因,用于疾病治疗. 这项技术也可以应用于有针对性地递送抗原以开发疫苗.
3。. 用于脓毒症治疗的新型纳米树脂
脓毒症是由感染性或非感染性源性扩散损伤引起的全身高炎症反应引起的. 脂多糖(LPS)在革兰氏阴性(GN)细菌感染引起的脓毒症中被认为是一种有效的致病性内毒素. 血液中的LPS与上皮细胞上的toll样受体-4 (TLR-4)结合, 单核细胞和巨噬细胞, 引发炎症细胞因子的大量产生, 在激活凝血和互补级联以及引起血管通透性增加和组织损伤方面,哪一种破坏性大于保护性. 病原体和受损细胞释放的病原体/损伤相关分子模式(PAMPs/DAMPs)进一步刺激炎症反应, 导致器官衰竭和死亡. 减轻脓毒症进展中的多重触发和介质可能有助于控制高炎症和降低死亡率, 鉴于单目标免疫调节疗法在临床试验中的失败.
类似于蛋白质封装, 我们可以通过协同和多价电荷和疏水相互作用有效地捕获端枝状纳米颗粒中的LPS(负电荷脂质结构)(图3). 即使在血清蛋白或多粘菌素B (PMB)存在的情况下,工程端突纳米载体也能与LPS强结合。, 一种黄金标准的强效lps粘合剂. 我们进一步将树突状纳米粒子固定在特定尺寸的水凝胶树脂上,通过血液灌流选择性和有效地去除LPS和细胞因子,以控制败血症(图3 b). 此外,这些纳米陷阱树脂还可以有效地清除DAMPs分子.g. 血浆中的无细胞DNA和血红素. Septic mice were induced by cecal ligation and puncture (CLP) procedure and cytokines in the septic blood can be efficiently removed by >95% after incubation with nanotrap resins. 进一步, 纳米捕集器树脂联合抗生素可有效治疗CLP小鼠,同时控制感染和炎症(图3 c & 3D).
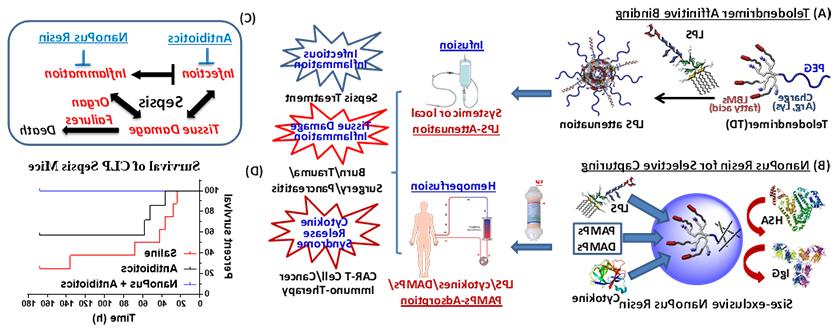
与其他血液灌流技术相比,在脓毒症治疗的对照临床试验中失败, e.g. PMB-based Toraymyxin® 用于去除LPS和疏水多孔Cytosorb® 非特异性细胞因子吸附, 我们的纳米陷阱树脂提供了一种“一体化”的方法来消除脓毒症血液中的内毒素、细胞因子和其他DAMPs/PAMPs分子. 除了, 纳米阱树脂的电荷可以根据患者的免疫状态选择性地清除促炎或抗炎细胞因子或同时清除两者. 将血液灌流转化为降低重症脓毒症死亡率的有效治疗方法,在临床上具有广阔的应用前景. 这种方法也有望用于治疗危重患者的心脏手术, 创伤, 有细胞因子风暴风险的烧伤或CAR - t细胞治疗. 最近,该项目得到了NIH/NIGMS R01基金的资助. 它很有希望转化为临床来挽救数百万严重脓毒症患者的生命.
2011年至今的刊物
- 王丽,季霞,郭东,石超,罗军. 表面固相合成具有良好定义的两性离子两亲体以增强抗癌药物的传递. 摩尔制药. 2021 june 7;18(6):2349-2359. doi: 10.1021 / acs.molpharmaceut.1c00163. 2021年5月13日. PubMed PMID: 33983742.
- 郭东,季霞,罗军. 面向肿瘤纳米治疗临床转化的合理纳米载体设计. 生物医学硕士. 2021年2月4日;. doi: 10.1088/1748 - 605 x / abe35a. [Epub ahead of print] PubMed PMID: 33540386.
- 石超,王旭,王磊,孟强,郭东,陈磊,戴敏,王刚,库尼瑞,罗军.*纳米陷阱通过减轻过度炎症提高严重败血症患者的生存率. Nat Commun. 2020;11(1):3384. PMID: 32636379. http://www.自然.com/articles/s41467 - 020 - 17153 - 0
- 郭,D.,史,C.王,L., Ji, X.张,S. & 罗,我.*合理设计胶束纳米载体,用于治疗银屑病的亲水性甲氨蝶呤的递送. 高分子材料学报,33 (2):448 - 448 (2020).
- Scheibel D.M.郭,D.罗,J. & Gitsov,我. 单一酶介导具有广泛生物医学潜力的多嵌段共聚物的“准活”形成. 生物大分子学报,21 (2):448 - 448 (2020).
- 王,我.,史,C.王,X.郭,D.邓肯,T。.M. & 罗,我. 具有明显功能差异的两性离子双面树突状分子增强蛋白质递送. 生物材料学报,2019,24 (5):119233,doi: 10.3969 / j.i ssn . 1001 - 1001.1016/j.生物材料.2019.119233. (IF: 10.273)
- 华盈元博大钟, 布莱恩Zeberl, 徐王*, 罗俊涛*聚合后修饰的组合方法用于治疗递送系统的合理开发, Acta Biomaterialia, 2018, doi: 10.1016/j.actbio.2018.04.010 (IF: 6.319)
- 徐王*, 常施, 丽丽王, 罗俊涛*细胞内蛋白质递送的聚阳离子-端枝状分子纳米复合物, 胶体和表面B:生物界面, 2018, 162: 405-414. id: 29247913 (if: 4).152)
- 罗纳德·J. 施罗德二,Jason Audlin,罗俊涛,Brian D. 尼古拉斯, 硫代硫酸钠在豚鼠淋巴管周围中耳内的药代动力学, 耳科学杂志, 2018, 13, 54-58.
- 贾永光,金佳红,刘萨,任丽,罗军涛,X. X. 朱, 主客识别合成低分子量聚乙烯醇自愈水凝胶, 《生物高分子, 2018, 19 (2), 626-632. id: 29341595 (if: 5).246)
- 丹丹郭, 常施, 王许, 丽丽王, 盛乐张, 罗俊涛*含核黄素的端突分子纳米载体高效递送阿霉素:高负载能力, 增加了稳定性, 提高抗癌效果, 生物材料, 2017, 141, 161-175. (IF: 8.387)
- 王丽丽,史长英,A福里斯特. 王旭,郭丹丹,王旭.H. Wojcikiewicz, 罗军涛*硼替佐米和阿霉素靶向共递送的多功能端突分子纳米载体,重新启动其在卵巢癌治疗中的协同作用, 癌症研究, 2017, 77(12), 3293-3305. id: 28396359 (if: 9).329)
- 王旭,石长英,张丽,林美云,郭丹丹,王丽丽,杨燕,Thomas M. 罗俊涛,Duncan, *基于结构的蛋白质递送纳米载体设计. 中文信息学报,2017,(6),267-271 (IF: 6).185)
- 克里斯汀•米. Burrer, Helen Au燃烧, Wang Xu, Luo Juntao, Fardokht A. 扎内塔·尼科洛夫斯卡-科尔斯卡,加里·C. 包裹成纳米颗粒的Chan Mcl-1小分子抑制剂对hcmv感染的单核细胞的杀伤效果增强. 抗病毒研究,2017,38 (8):40-46. id: 27914937 (if: 4).909)
- 王许, Alexa博德曼, 常施, 丹丹郭, 丽丽王, 沃尔特·A·霍尔, 可调脂质-端突混合纳米颗粒在脑肿瘤治疗中的细胞内蛋白递送. SMALL. 2016, 12(31), 4185-4192. id: 27375237 (if: 8.643)
- 王许, 常施, 李张, Alexa博德曼, 丹丹郭, 丽丽王, 沃尔特·A·霍尔, Stephan主教练威尔肯斯, 罗军涛*亲和控制蛋白在亚30nm远端分子纳米载体上的多价和协同相互作用. 生物材料. 2016, 101: 258–271. id: 27294543 (if: 8.387)
- Wenjuan江, 孝义王, 丹丹郭, Juntao罗, Shikha Nangia对阿霉素有效包封的端突结构药物特异性设计. 物理化学学报,2016,36 (6),976 - 777,PMID: 27513183 (IF: 1).187)
- Wenjuan江; Juntao罗; Shikha Nangia. 多尺度方法研究抗癌药物端突分子纳米载体的自组装. 朗缪尔. 2015, 31(14):4270-80. 预期值:25532019(如果:3).993)
- 常施; 丹丹郭; Kai Xiao; 王许; 丽丽王; Juntao罗* A drug-specific nanocarriers design for efficient anti癌症 therapy. 自然通讯. 2015, 9; 6: 7449. PMID: 26158623. (IF: 11.329; citations: 53)
- Gaofei徐, 常施, 丹丹郭, 丽丽王, 云灵, Xiaobing汉, 罗俊韬*功能分离的含香豆素的端突分子纳米载体用于结肠癌治疗的SN-38的高效递送. Acta Biomaterialia. 2015, 21:85-98. id: 25910639 (if: 6.025)
- Wenzhe黄, 王许, 常施, 丹丹郭, Gaofei徐, 丽丽王, Alexa博德曼, 罗俊涛*微调含维生素e的端突分子,用于结肠癌治疗中藤黄酸的有效输送. 分子制药学. 2015, 12(4):1216-29. id: 25692376 (if: 4).384)
- Liqiong Cai; Gaofei徐; 常施; 丹丹郭; 王许; Juntao罗* Telodendrimer Nanocarrier for Co-delivery of Paclitaxel and Cisplatin: A Synergistic Combination Nanotherapy for Ovarian Cancer Treatment. 生物材料. 2015, 37C:456-468. id: 25453973 (if: 8.387; citations: 62)
- Yu Shao; 常施; Gaofei徐; 丹丹郭; Juntao罗* A photo and redox dual responsive reversibly crosslinked nanocarrier for efficient tumor-targeted 药物输送. ACS应用材料与接口. 2014, 6(13), 10381-92. id:24921150 (if: 7.504; citations: 52)
- 常施; Dekai Yuan; Shikha Nangia; Gaofei徐; 丹丹郭; Kit S. 林; Juntao罗* Structure-property relationships study of a well-defined telodendrimer to improve the hemocompatibility of nanocarriers for anti癌症 药物输送. 水土保持学报,2014,30 (23),6878-6888. id: 24849780 (if: 3.993)
- Yu Shao; Yong-Guang Jia; 常施; Juntao罗; X. X. 朱, 嵌段和无规共聚物承载胆酸和低聚乙二醇悬垂基团:聚集, Thermosensitivity, 和药物装载. 生物大分子,2014,15 (5),pp 1837-1844. id:24725005 (if: 5).750)
- Yung-Shin Sun; Yiyan Fei; Juntao罗; Seth Dixon; James P. Landry; Kit S. 林; X.D. 利用单头单化合物合成化合物文库生成小分子微阵列,用于无标记检测和发现针对蛋白质靶点的小分子配体. 综合通信,2014,44(7),987-1001. (IF: 1.065)
- Wei He; Juntao罗; Feliza Bourguet; Li Xing; Sun K. Yi; Tingjuan Gao; Craig Blanchette; Paul T. Henderson; Edward Kuhn; Mike Malfatti; William J. Murphy; R. Holland Cheng; Kit S. 林; Matthew A. 科尔曼. 控制直径, 单分散性, ApoA1纳米脂蛋白颗粒的溶解性. 蛋白质科学. 2013, 22 (8), 1078-1086. id: 23754445 (if: 3).039)
- 尼古拉斯 J. Kenyon; Jennifer M. Bratt; Joyce Lee; Juntao罗; Lisa M. Franzi; Amir A. Zeki; Kit S. 林. 含地塞米松的自组装纳米颗粒作为过敏性气道炎症的新疗法. 科学通报,2013,26 (4):779 - 779. id: 24204939 (if: 3).234)
- Tzu-Yin Lin; Yuanpei Li; Hongyong Zhang; Juntao罗; Neal Goodwin; Tingjuan Gao; Ralph De Vere White; Kit S. 林; Chong-Xian Pan. 肿瘤靶向多功能胶束在晚期膀胱癌影像学和化疗中的应用. 纳米(Lond). 2013, 8, 1239-1251. id: 23199207 (if: 4).889)
- Yung-Shin Sun; Juntao罗; Kit S. 林; X.D. 朱. 斜入射反射率差显微法检测胶束的形成和解体. 科学仪器 & 科技进步,2013,41 (1):545-555. (IF: 1.433)
- Wenzhe黄; 常施; Yu Shao; Kit S. 林; Juntao罗* The Core-Inversible Micelles for Hydrophilic Drug Delivery. 化学通讯,2013,49,6674-6676. id:23775217 (if: 6).567,引文11)
- Yu Shao; Wenzhe黄; 常施; Sean T Atkinson; Juntao罗*. 可逆交联纳米载体在癌症治疗中按需给药. 中华医学杂志,2012,31 (3):1409-1427. PMID: 23323559(来源:33)
- 文武肖, Juntao罗*, 保罗·亨德森,Tessta耆那教徒的, 约翰Wriggs, 哈利曾, 祁绍林*, 高分子纳米胶束及载药化疗药物在小鼠卵巢癌异种移植模型上的分布, 国际纳米医学杂志, 2012, 7: 1587–1597. (*通讯作者)PMID: 22605931.383,引文28)
- Kai Xiao; Yuanpei Li; Joyce S. Lee; Abby M. Gonik; Tiffany Dong; Gabriel Fung; Eduardo Sanchez; Li Xing; Holland R. Cheng; Juntao罗*; 祁绍林*. “OA02”肽促进了紫杉醇负载胶束纳米颗粒在体内对卵巢癌的精确靶向, 癌症研究, 2012, 72, 2100-2010. (*通讯作者)PMID:22396491.329; citations: 71)
- Yuanpei Li; 文武肖; Kai Xiao; Lorenzo Berti; Juntao罗*; Harry P. Tseng; Gabriel Fung; 祁绍林*. 定义良好的, 可逆硼酸盐交联纳米载体对pH和顺式二醇的靶向药物递送, 安吉旺特化学国际版, 2012, 51(12), 2864-2869. (*通讯作者)PMID:22253091.709; citations: 270)
............这项工作在2012年安吉旺特化学国际版的一周内封底上被强调为最重要的论文(MIP), 51(12), 3027. 该研究在《治疗传递》杂志2012年3期(3),303-306上作为新闻报道. - 李元培,Madhu S. 罗俊涛,肖文武,罗俊涛. Voss和Kit S. 林, 纳米粒子与血液蛋白相互作用过程中组装结构和动力学的探测. 生物质化学工程,2012,6 (11),9485-9495. id: 23106540 (if: 13.334; citations: 40)
- Tzu-yin Lin; Hongyong Zhang; Juntao罗; Yuanpei Li; Tingjuan Gao; PN Lara Jr, Ralph de Vere White; Kit S 林; Chong-Xian Pan. 多功能靶向胶束纳米载体对膀胱癌的成像和治疗潜力. 国际纳米医学杂志,2012,7,2793-2804. id: 22745542 (if: 4.383)
- Jason Kato; Yuanpei Li; Kai Xiao; Joyce S. Lee; Juntao罗; Joseph M. Tuscano; Robert T. O'Donnell; KitS. 林. 二硫交联胶束靶向传递长春新碱到b细胞淋巴瘤, 分子制药学. 2012, 9(6):1727-1735. id: 22530955 (if: 4).384)
- Hongyong Zhang; Juntao罗; Yuanpei Li; Paul T. Henderson; Yanchun Wang; Sebastian Wachsmann-Hogiu; Weixin Zhao; Kit S. 林; Chong-xian Pan. 高亲和肽的特性及其在靶向白血病干细胞的纳米治疗中的可行性, 纳米, 2012, 8(7):1116-24. id:22197725 (if: 4.889)
- Noriko Satake; Joyce Lee; Kai Xiao; Juntao罗; Susmita Sarangi; Astra Chang; Bridget McLaughlin; Ping Zhou; Elaina Kenney; Liliya Kraynov; et al. 纳米颗粒靶向治疗儿童急性淋巴细胞白血病, 国际光学工程学会会刊, 2011;8031:[80311U].
- Kai Xiao; Juntao罗 *; Yuanpei Li; Joyce S. Lee; Abby M. Gonik; Gabriel Fung; Kit S. 林*. 聚乙二醇-低胆酸端突胶束靶向递送阿霉素至b细胞淋巴瘤, 控释杂志, 2011, 155(2), 272-281. (*通讯作者)PMID:21787818.705,引文100)
- Yuanpei Li; Kai Xiao; Juntao罗*; 文武肖; Joyce S. Lee; Abby M. Gonik; Jason Kato; Tiffany Dong; Kit S. 林*. 定义良好的, 按需递送紫杉醇的可逆二硫交联胶束, 生物材料, 2011, 32(27), 6633-6645. (*通讯作者)PMID:21658763 (IF: 8.387; citations: 226)

